二氧化硫|每日打卡 2022高考倒计时226天!

文章图片

文章图片
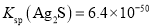
文章图片

文章图片
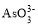
文章图片

文章图片

文章图片

文章图片

文章图片
三氧化二砷(As2O3)可用于治疗急性早幼粒白血病 。 利用某酸性含砷废水(含、H+、)可提取三氧化二砷 , 提取工艺流程如下:
已知:①常温下 , ; 。 【二氧化硫|每日打卡2022高考倒计时226天!】②As2O3+6NaOH=2Na3AsO3+3H2O 。
③As2S3易溶于过量的Na2S溶液中 , 故加入FeSO4的目的是除去过量的S2- 。
回答下列问题:
(1)操作M的名称是________ , 滤液N中含有的阳离子有Fe2+、H+、________ 。
(2)“焙烧”操作中 , As2S3参与反应的化学方程式为____________ 。
(3)“碱浸”的目的是_____________ , “滤渣Y”的主要成分是_____________(写化学式) 。
(4)“氧化”中发生反应的离子方程式为___________________ 。
(5)该流程中可循环使用的物质是_________(写化学式) , 某次“还原”过程中制得了1.98kgAs2O3 , 则消耗标准状况下该物质的体积是________L 。
(6)溶液中金属离子的除去方法之一是Na2S沉降法 。 常温下 , 若某溶液中含Fe2+、Ag+ , 且浓度均为0.1mol·L-1 , 则向该溶液中滴加稀Na2S溶液时 , 先生成的沉淀是________(填化学式) 。
【答案】
过滤 Na+从As2O3和Fe2O3的混合物中分离出As元素 Fe2O3SO2 448 Ag2S【解析】
酸性含砷废水(含、H+、)加入Na2S和FeSO4得到As2S3和FeS沉淀 , 过滤将沉淀和滤液分离;As2S3和FeS在空气中焙烧得到As2O3、Fe2O3以及SO2 , 加入NaOH溶液溶解焙烧产物 , As2O3反应生成Na3AsO3形成溶液 , 过滤得到的滤渣Y为Fe2O3 , 加入双氧水将Na3AsO3氧化得到Na3AsO4 , 通入二氧化硫和稀硫酸将Na3AsO4还原得到As2O3 。(1)将固体和液体分离可以采用过滤的方法;沉砷时加入了硫化钠和硫酸亚铁 , 所以阳离子除了Fe2+、H+还有Na+;
(2)焙烧过程中As2S3中S元素被空气中的氧气氧化为SO2 , 结合元素守恒和电子守恒可得反应方程式为;(3)根据题目所给信息可知As2O3可以和NaOH溶液发生反应 , 而Fe2O3不能 , 所以碱浸的目的是从As2O3和Fe2O3的混合物中分离出As元素;滤渣Y为Fe2O3;
(4)氧化过程中被双氧水氧化成 , 结合电子守恒和电荷守恒可得离子方程式为;
(5)焙烧过程产生二氧化硫 , 二氧化硫具有还原性 , 还原时可用二氧化硫还原Na3AsO4 , 所以可以循环使用的物质为SO2;1.98kgAs2O3的物质的量为=10mol , 还原过程中As元素由+5价变为+2价 , 所以生成10mol产品转移40mol电子 , S元素由+4(SO2)价变为+6(SO)价 , 所以转移40mol电子时需要消耗20mol二氧化硫 , 标况下体积为448L;
推荐阅读
- 电工|看完这些电工考试题库,C位王者就是你!(每日都会持续更新哦)
- 科普|江西东乡王桥中学:科技馆成为“双减”打卡地
- 国企|国企一个办公室里,为什么只让我们仨考进来的打卡考勤呢?
- 老人|【2022高考倒计时149天】同时风华正茂 何甘他人之后
- |【每日一词】“决定权”的英文表达
- A-Level|元旦小长假干点啥?不如去这几所青岛国际学校打卡!
- 西北师范大学|甘肃省2所高校参加传统体育专业招生,考前17天起考生每天要健康打卡
- 班级|快乐奔跑 健康成长!德城区中小学生每日跑步强体魄
- 站厅|复旦大学站到了!18号线今天通车,还能乘到上海财经大学,一起来打卡!
- 评价|每日真题 | 22教育学考研——真题精炼Day66











